Онко подмечено: анализ РНК опухоли поможет выбрать эффективный препарат
Как медики продлевают жизнь пациентов с раком на самых тяжелых стадиях болезни

EN

Российские медики разработали специальный алгоритм, который автоматически анализирует результаты РНК-секвенирования раковых клеток и определяет, какой препарат лучше всего подойдет конкретному пациенту. Сегодня персонализированную терапию получают только 15–20% больных со злокачественными образованиями. Новый подход позволит применять таргетные лекарственные средства практически для всех больных. По мнению экспертов, на данный момент уже создано достаточное количество эффективных препаратов от рака, и для успешного лечения решающим становится выбор наиболее подходящих.
Алгоритм для назначения таргетных препаратов
Специалисты Института персонализированной онкологии Сеченовского университета начали применять на практике новый алгоритм, который позволяет на основании анализа результатов РНК-секвенирования образцов раковой опухоли назначать пациенту наиболее подходящий таргетный препарат. Разработка была создана при участии сотрудников МФТИ и других российских исследовательских организаций.

До последнего времени лекарственные средства, нацеленные на отдельные мишени, назначали только тем больным, у которых находили диагностические мутации в ДНК. Однако это только 15–20% пациентов с раком, так как у остальных этих маркеров просто не обнаруживали. Новый подход сделает таргетную терапию доступной практически для всех онкобольных.
— Подбор терапии на основе профилей РНК существенно повышает шанс найти действительно эффективное лечение для индивидуального больного. Рутинно используемый сегодня подбор лечения на основе диагностических мутаций ДНК полезен лишь для 15–20% онкопациентов, так как у остальных в опухоли таких мутаций попросту не оказывается. Определение тактики лечения на основе анализа РНК будет полезно практически для всех пациентов. Внедрение этой технологии поможет увеличить продолжительность жизни десятков тысяч больных с опухолями поздних стадий, — сказал главный научный сотрудник Института персонализированной онкологии Сеченовского университета, профессор РАН Антон Буздин.

Изучение экспрессии генов опухоли с помощью РНК-секвенирования показывает, молекулярные мишени каких противораковых препаратов будут активны для конкретной опухоли, а каких — неэффективны. Алгоритм выявляет измененную активность генов-мишеней и молекулярных путей и из множества существующих противоопухолевых средств подбирает те, которые будут максимально эффективны для конкретного пациента. Результат анализа предоставляется в виде рейтинга более чем из 170 лекарств.

Для оценки возможностей алгоритма было проведено клиническое исследование с участием 239 взрослых пациентов с развитыми злокачественными, преимущественно метастатическими опухолями. 135 из них получали лекарственную терапию, остальные проходили паллиативное лечение или лучевую терапию. 59% участников назначали лечение по рекомендации алгоритма, а остальные лечились по стандартным протоколам.
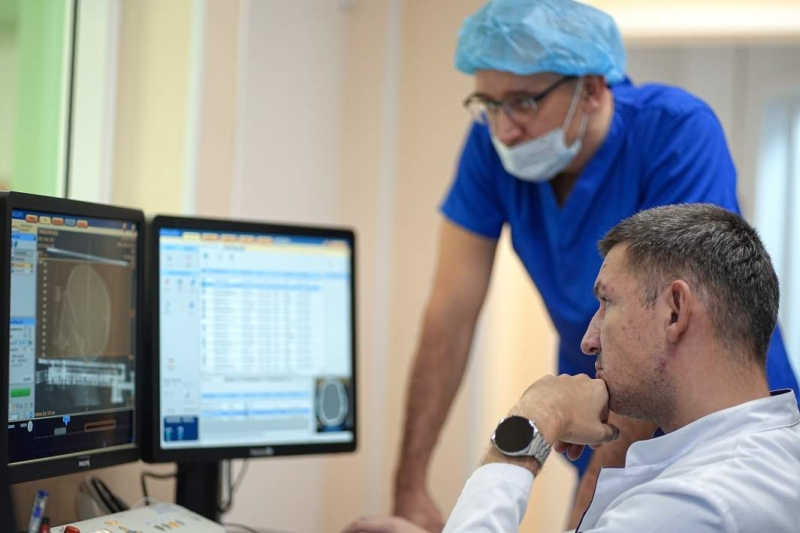
При этом те, кому назначили лечение на основе индивидуальных рейтингов, в среднем имели более высокую тяжесть заболевания. Однако именно у этих пациентов зафиксировали более длительную беспрогрессивную выживаемость (время, за которое болезнь не прогрессирует).
Эффективность на последних стадиях рака
В целом результаты клинического исследования подтвердили, что подбор противораковой терапии на основе анализа РНК опухоли позволяет почти в два раза повысить вероятность ответа на терапию на поздних стадиях рака, а также увеличить безрецидивный период в среднем на 10 месяцев.
— Следует отметить, что речь здесь идет в основном про больных на четвертой стадии рака, имеющих метастазы. То есть это наиболее тяжелая группа больных. И даже в этой группе алгоритмически подобранная терапия показала весьма высокую эффективность, — добавил Антон Буздин.
Сегодня в результате упорных трудов ученых, исследователей, фармацевтов, технологов, врачей уже создано немало лекарственных препаратов против рака. Если они по результатам исследований обладают надлежащим качеством и показали свою эффективность, значит, средство реально эффективно. Но если пациенту оно не помогает, скорее всего, вопрос не в том, что лекарство не работает, а в том, что это не тот препарат, который должен быть использован в данной ситуации, отметил заведующий лабораторией анализа показателей здоровья населения МФТИ Станислав Отставнов.
— Сегодняшние стандарты лечения, к сожалению, пока не в полной мере учитывают возможности персонализированной терапии. И предстоит еще сделать немало, чтобы ее активнее применяли, но это единственно правильный путь. На самом деле нет неэффективных препаратов, есть не вполне обоснованные назначения, и это даже не ошибка отдельного врача, а ошибка всей системы — только широкое внедрение персонализированной медицины поможет нам решить проблему, — сказал Станислав Отставнов.

Технологии полногеномного секвенирования уже долгое время применяются в США и Европе. Спектр параметров, которые учитываются при анализе, постоянно расширяется, и сейчас тестируют до 600 показателей. В России многие лаборатории пытаются делать что-то похожее. Их успех будет зависеть от перечня анализируемых генов. Появление нового алгоритма можно только приветствовать, главное — чтобы результаты его использования были так же достоверны, как и за рубежом, отметил главный врач-онколог Европейской клиники хирургии и онкологии Андрей Пылев.


